Jenis / Macam-macam Reaksi Senyawa Hidrokarbon, Oksidasi, Substitusi, Adisi, Eliminasi, Contoh, Pengertian - Pada senyawa-senyawa hidrokarbon (alkana, alkena, alkuna) sanggup terjadi reaksi-reaksi, menyerupai reaksi oksidasi, reaksi adisi, reaksi substitusi, dan reaksi eliminasi. Pada subbab ini, Anda akan mempelajari reaksi-reaksi tersebut.
1. Reaksi Oksidasi pada Senyawa Hidrokarbon
Suatu senyawa alkana yang bereaksi dengan oksigen menghasilkan karbon dioksida dan air disebut dengan reaksi pembakaran. Perhatikan persamaan reaksi oksidasi pada senyawa hidrokarbon berikut.
CH4(g) + O2(g) → CO2(g) + H2O(g)
Reaksi pembakaran tersebut, intinya merupakan reaksi oksidasi. Pada senyawa metana (CH4) dan karbon dioksida (CO2) mengandung satu atom karbon. Kedua senyawa tersebut harus mempunyai bilangan oksidasi nol maka bilangan oksidasi atom karbon pada senyawa metana yaitu –4, sedangkan bilangan oksidasi atom karbon pada senyawa karbon dioksida yaitu +4.
Bilangan oksidasi atom C pada senyawa karbon dioksida meningkat (mengalami oksidasi), sedangkan bilangan oksidasi atom C pada senyawa metana menurun.
2. Reaksi Substitusi pada Senyawa Hidrokarbon
Reaksi substitusi merupakan reaksi penggantian gugus fungsi (atom atau molekul) yang terikat pada atom C suatu senyawa hidrokarbon.
Pada reaksi halogenasi alkana, atom hidrogen yang terikat pada atom C senyawa alkana digantikan dengan atom halogen. Ketika gabungan metana dan klorin dipanaskan sampai 100°C atau radiasi oleh sinar UV maka akan dihasilkan senyawa klorometana, menyerupai reaksi berikut.
100 °C | ||
CH4(g) + Cl2(g) | → | CH3Cl(g) + HCl(g) |
Jika gas klorin masih tersedia dalam campuran, reaksinya akan berlanjut menyerupai berikut.
100 °C | ||
CH3Cl(g) + Cl2(g) | → | CH2Cl2(g) + HCl(g) |
100 °C | ||
CH2Cl2(g) + Cl2(g) | → | CHCl3(g) + HCl(g) |
100 °C | ||
CHCl3(g) + Cl2(g) | → | CCl4(g) + HCl(g) |
Reaksi substitusi tersebut dipakai dalam pembuatan senyawa diklorometana. Jika reaksi dilakukan pada senyawa etana, reaksi akan menghasilkan dikloroetana. Diklorometana dipakai untuk pengelupasan cat, sedangkan triklorometana dipakai untuk dry–clean.
3. Reaksi Adisi pada Senyawa Hidrokarbon
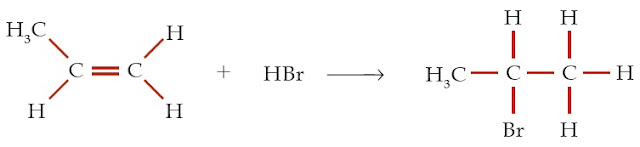
Jika senyawa karbon mempunyai ikatan rangkap dua (alkena) atau rangkap tiga (alkuna) dan pada atom-atom karbon tersebut berkurang ikatan rangkapnya, lalu digantikan dengan gugus fungsi (atom atau molekul). Reaksi tersebut dinamakan reaksi adisi. Perhatikan reaksi antara 1-propena dengan asam bromida menghasilkan 2-bromopropana sebagai berikut.
Hidrokarbon yang mempunyai ikatan rangkap dua atau rangkap tiga merupakan senyawa tak jenuh. Pada senyawa tak jenuh ini memungkinkan adanya penambahan atom hidrogen. Ketika suatu senyawa tak jenuh direaksikan dengan hidrogen halida maka akan menghasilkan produk tunggal.
4. Reaksi Eliminasi pada Senyawa Hidrokarbon
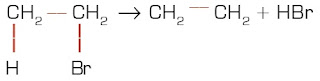
Reaksi eliminasi merupakan reaksi kebalikan dari reaksi adisi. Reaksi eliminasi melibatkan pelepasan atom atau gugus atom dari sebuah molekul membentuk molekul baru. Contoh reaksi eliminasi yaitu eliminasi etil klorida menghasilkan etana dan asam klorida.
C2H5Cl(aq) → C2H4(aq) + HCl(aq)
Reaksi eliminasi terjadi pada senyawa jenuh (tidak mempunyai ikatan rangkap) dan menghasilkan senyawa tak jenuh (memiliki ikatan rangkap).
Contoh Soal 1 :
Contoh Soal 1 :
Diketahui reaksi senyawa karbon:
CH4(g) + Cl2(g) → CH3Cl(g) + HCl(g)
CH4(g) + CH2Br(g) → CH2 ─ CH2(g) + HBr(g)Kedua reasi tersebut termasuk jenis reaksi ....
A. adisi dan substitusi
B. adisi dan eliminasi
C. substitusi dan adisi
D. substitusi dan eliminasi
E. eliminasi dan adisi
Kunci Jawaban :
Reaksi substitusi: reaksi penukaran unsur.
Contoh:
H3C ─ H + Cl ─ Cl → H3CCl + HCl
Reaksi eliminasi: perubahan senyawa jenuh menjadi tak jenuh, pembentukan ikatan tunggal menjadi rangkap.
Anda kini sudah mengetahui Reaksi Senyawa Hidrokarbon. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Rahayu, I. 2009. Mudah Belajar Kimia, Untuk Kelas X Sekolah Menengah Atas/Madrasah Aliyah. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p 210.