Pengertian Afinitas Elektron Unsur Kimia, Cara Menentukan, Satu Golongan, Periode - Afinitas elektron ialah besarnya energi yang dibebaskan satu atom netral dalam wujud gas pada waktu mendapatkan satu elektron sehingga terbentuk ion negatif.
a. Dalam satu golongan dari atas ke bawah afinitas elektron semakin kecil.
b. Dalam satu periode dari kiri ke kanan afinitas elektron semakin besar.
Penjelasan:
a. Apabila ion negatif yang terbentuk stabil, energi dibebaskan dinyatakan dengan tanda negatif (-). Apabila ion negatif yang terbentuk tidak stabil, energi diperlukan/diserap dinyatakan dengan tanda positif (+).
b. Kecenderungan dalam afinitas elektron lebih bervariasi dibandingkan dengan energi ionisasi.
Tabel 1. Harga Afinitas Elektron Beberapa Unsur (kJ)/mol)
Li | 60,4 | B | 27 | C | 123 | N | 7 | O | 142,5 | F | 331,4 |
Na | 52,2 | Al | 45 | Si | 135 | P | 72,4 | S | 202,5 | Cl | 352,4 |
K | 48,9 | Ga | 30 | Ge | 120 | As | 178 | Se | 197 | Br | 327,9 |
Rb | 47,7 | In | 29 | Sn | 122 | Sb | 102 | Te | 192,1 | I | 298,4 |
Cs | 46,0 | Tl | 30 | Pb | 110 | Bi | 110 | Po | 190 | At | 270 |
Unsur-unsur halogen (Gol. VII A) memiliki afinitas elektron paling besar/paling negatif yang berarti paling gampang mendapatkan elektron. Kecenderungan afinitas elektron menunjukkan contoh yang sama dengan contoh kecenderungan energi ionisasi.
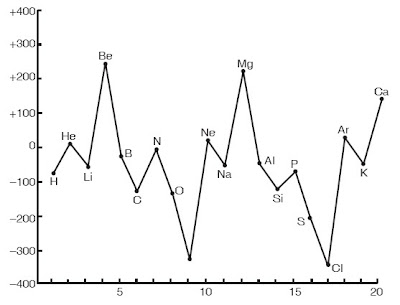 |
| Gambar 1. Grafik kecenderungan afinitas elektron 20 unsur pertama dalam TPU. |
Anda kini sudah mengetahui Afinitas Elektron. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Setyawati, A. A. Kimia : Mengkaji Fenomena Alam Untuk Kelas X SMA/MA. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 186.





