Pengertian Persamaan Reaksi Kimia, Contoh, Syarat-syarat, Aturan, Koefisien Reaksi - Persamaan reaksi yakni persamaan yang menggambarkan korelasi zat-zat kimia yang terlibat sebelum dan sehabis reaksi kimia. Persamaan reaksi dinyatakan dengan rumus kimia zat-zat yang bereaksi dan hasil reaksi, angka koefisien, dan fase/wujud zat. [1]
Zat-zat yang bereaksi disebut pereaksi/reaktan dituliskan di sebelah kiri tanda anak panah, sedangkan zat-zat hasil reaksi atau produk reaksi dituliskan di sebelah kanan tanda anak panah. [1]
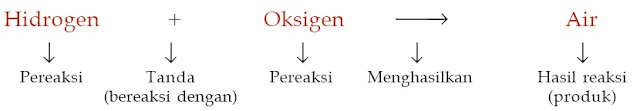
Suatu persamaan reaksi kimia sanggup ditulis dengan dua cara, yaitu persamaan perkataan dan persamaan simbol. Persamaan perkataan yakni persamaan kimia yang memberi nama pereaksi-pereaksi dan nama hasil reaksinya, contohnya hidrogen bereaksi dengan oksigen menghasilkan air.
Persamaan simbol yakni suatu akronim dalam menguraikan suatu reaksi kimia. Simbol ini memakai rumus kimia dari pereaksi-pereaksi dan hasil reaksi, serta memakai tanda tambah (+) dan tanda panah (→). Persamaan reaksi ini menggambarkan korelasi zat-zat yang terlibat sebelum dan sehabis reaksi, baik secara kualitatif maupun secara kuantitatif.
Perubahan dari pereaksi menjadi hasil reaksi digambarkan dengan tanda anak panah. Angka koefisien menyatakan jumlah partikel dari setiap pereaksi dan hasil reaksi. Angka koefisien dituliskan di depan rumus kimia zat, supaya reaksi menjadi setara. Reaksi dikatakan setara bila jumlah atom di kiri sama dengan jumlah atom di kanan tanda anak panah, sehingga sesuai dengan Hukum Kekekalan Massa. [1]
Contoh: natrium hidroksida direaksikan dengan asam klorida menghasilkan natrium klorida dan air.
Maka persamaan reaksinya:
natrium hidroksida + asam klorida → natrium klorida + air
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O (aq)
NaOH dan HCl disebut pereaksi/reaktan
NaCl dan H2O disebut hasil reaksi
Persamaan reaksi yang tepat disebut juga persamaan reaksi yang telah setara. Syarat-syarat persamaan reaksi setara sebagai berikut. [2]
- Jenis unsur-unsur sebelum dan sehabis reaksi selalu sama.
- Jumlah masing-masing atom sebelum dan sehabis reaksi selalu sama (memenuhi aturan kekekalan massa).
- Perbandingan koefisien reaksi menyatakan perbandingan mol (khusus yang berwujud gas perbandingan koefisien juga menyatakan perbandingan volume asalkan suhu dan tekanannya sama).
- Pereaksi dan hasil reaksi dinyatakan dengan rumus kimia yang benar.
- Wujud zat-zat yang terlibat reaksi harus dinyatakan dalam tanda kurung setelah rumus kimia.
Untuk menciptakan persamaan reaksi menjadi setara diperbolehkan mengubah jumlah rumus kimia (jumlah molekul atau satuan rumus), tetapi dihentikan mengubah rumus kimia zat-zat yang terlibat persamaan reaksi. Jumlah satuan rumus kimia disebut koefisien. [2]
Berikut ini yakni klarifikasi mengenai aturan persamaan reaksi kimia : [3]
Persamaan reaksi menyatakan kesetaraan jumlah zat-zat yang bereaksi dengan jumlah zat-zat hasil reaksi. Unutuk menyatakannya dipakai rumus kimia zat-zat, koefisien reaksi, dan wujud zat. Perhatikan teladan berikut:
2Na (s) + Cl2 (g) → 2NaCl (s)
a. Rumus kimia zat-zat
Zat-zat yang terlibat dalam reaksi kimia dinyatakan oleh rumus kimianya. Rumus pereaksi diletakkan di ruas kiri dan hasil reaksi diletakkan di ruas kanan. Kedua ruas dihubungkan oleh tanda panah yang menyatakan arah reaksi.
b. Koefisien reaksi
Koefisien reaksi menyatakan jumlah partikel dari setiap pereaksi dan produk reaksi. Pada teladan di atas, 2 molekul Na bereaksi dengan 1 molekul Cl2 menghasilkan 2 molekul NaCl. Koefisien reaksi 1 umumnya tidak ditulis.
Koefisien reaksi diberikan supaya persamaan reaksi sesuai dengan Hukum Kekekalam Massa dari Lavoisier, yang menyatakan bahwa:
“ Massa zat sebelum dan sehabis reaksi yakni sama”
Karena massa suatu zat berbanding lurus dengan jumlah partikel (atom), maka aturan tersebut sanggup pula berarti :
Jumlah atom dari setiap unsur di ruas kanan = Jumlah atom dari setiap unsur di ruas kiri
c. Wujud zat
Meskipun bukan keharusan, terkadang kita perlu mencantumkan wujud zat-zat yang terlibat dalam suatu reaksi. Wujud zat ditulis dengan akronim dalam tanda kurung, sebagai subskrip di belakang rumus kimia zat yang bersangkutan.
Tabel 1 .Penulisan Wujud Zat
Wujud Zat | Subskrip |
Padat (solid) | s |
Cair (liquid) | l |
Gas (gas) | g |
Larut dalam air (aqueous) | aq |
Lalu bagaimanakah cara menulis dan menyamakan persamaan reaksi kimia? Baca : Cara Menulis dan Menyetarakan Persamaan Reaksi Kimia.
Anda kini sudah mengetahui Reaksi Kimia. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Rahayu, I. 2009. Mudah Belajar Kimia, Untuk Kelas X Sekolah Menengah Atas/Madrasah Aliyah. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p 210.
Referensi Lainnya :
[1] Harnanto, A. dan Ruminten. 2009. Kimia 1 : untuk SMA/MA Kelas X. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 194.
[2] Setyawati, A. A. Kimia : Mengkaji Fenomena Alam Untuk Kelas X SMA/MA. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 186.
[3] Permana, I. 2009. Memahami Kimia 1 : SMA/MA untuk Kelas Semester 1 dan 2. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 175.