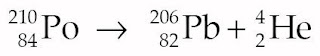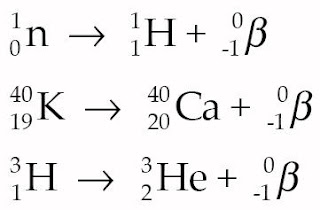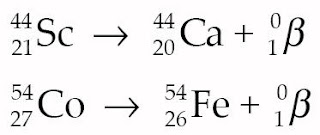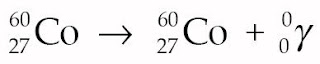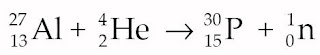fisika-dan-kimia-unsur-radioaktif" target="_blank">Sifat Fisika dan Kimia Unsur Radioaktif, Contoh Soal, Rumus, Defek Massa, Energi Ikat Inti Atom - Sifat Fisika dan Kimia Unsur Radioaktif yakni sebagai berikut :
a. Sifat-Sifat Fisika Unsur Radioaktif
Inti atom terdiri atas neutron. Massa suatu inti selalu lebih kecil dari jumlah massa proton dan neutron. Selisih antara massa inti yang bekerjsama dan jumlah massa proton dan neutron penyusunnya disebut defek massa.
Contoh Soal 1 :
Massa sebuah atom  yang ditentukan dengan spektrograf massa yakni 4,002603 sma. Massa proton 1,007277 sma, massa elektron 0,0005486 sma, dan massa netron 1,008665 sma.
yang ditentukan dengan spektrograf massa yakni 4,002603 sma. Massa proton 1,007277 sma, massa elektron 0,0005486 sma, dan massa netron 1,008665 sma.
Penyelesaian :
Massa atom  terhitung adalah:
terhitung adalah:
= (2 × 0,0005486 sma) + (2 × 1,007277 sma) + (2 × 1,008665 sma)
= 4,032981 sma
Defek massa = 4,032981 sma - 4,002603 sma = 0,030378 sma
Defek massa ini yakni ukuran energi pengikat neutron dan proton. Energi pengikat inti merupakan energi yang diharapkan untuk menguraikan inti (energi yang dilepaskan jikalau inti terbentuk). Energi pengikat inti sanggup dihitung dengan mengalikan defek massa dalam satuan massa atom per nukleon dengan faktor konversi massa energi yang besarnya 932 MeV/sma.
Contoh Soal 2 :
Atom  mengandung 26 proton, 30 neutron, dan 26 elektron.
mengandung 26 proton, 30 neutron, dan 26 elektron.
Massa dari partikel-partikel ini yakni :
p = 1,007277 sma
n = 1,008665 sma
e = 0,0005486 sma
Pembahasan :
Massa  menurut perhitungan yakni :
menurut perhitungan yakni :
= (26 × 1,007277 sma) + (30 × 1,008665 sma) + (26 × 0,0005486 sma)
= 56,4634 sma
Massa  menurut pengamatan yakni 55,9349 sma.
menurut pengamatan yakni 55,9349 sma.
Defek massa = 56,4634 sma – 55,9349 sma = 0,5285 sma
Energi pengikat inti  adalah :
adalah :
= 0,5285 × 932 = 492,56 MeV/sma
Energi pengikat inti  per nukleon yakni :
per nukleon yakni :
492,56 / 56 = 8,796 MeV/nukleon
Jadi, energi pengikat inti  adalah 8,796 MeV/nukleon.
adalah 8,796 MeV/nukleon.
Jika energi pengikat inti per nukleon disalurkan terhadap bilangan massa (A) akan diperoleh grafik menyerupai terlihat pada Gambar 1. berikut.
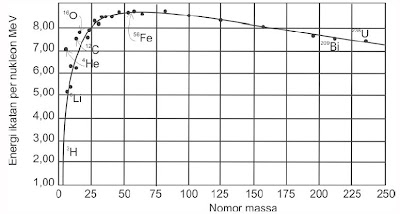 |
| Gambar 1. Grafik Energi Pengikat Inti Per Nukleon Terhadap Nomor Massa (Sumber: Kimia Universitas). |
Energi ikatan pernukleon terbesar untuk inti-inti dengan nomor massa sekitar 60 (besi dan nikel). Ini sanggup dilihat pada Gambar 1. bahwa puncak kurva mendekati  (besi).
(besi).
Hal ini terkait dengan kestabilan yang besar dari inti-inti unsur-unsur tersebut.
b. Sifat-Sifat Kimia Unsur Radioaktif
1) Mengalami Peluruhan Radioaktif
Unsur-unsur radioaktif sanggup mengalami aneka macam peluruhan yaitu, sebagai berikut.
a) Peluruhan alfa
Peluruhan alfa atau radiasi alfa terdiri dari pancaran inti atom helium yang disebut partikel alfa dinyatakan dengan  . Setelah terpancar di udara, partikel alfa bertabrakan dengan molekul udara yang netral.
. Setelah terpancar di udara, partikel alfa bertabrakan dengan molekul udara yang netral.
Partikel alfa tidak sanggup menembus kulit manusia, tetapi sanggup merusak kulit.
Contoh :
b) Peluruhan beta
Pada peluruhan ini, neutron bermetamorfosis proton. Pada proses ini tidak terjadi perubahan jumlah nukleon. Ada tiga macam peluruhan beta.
(1) Peluruhan negatron
Di sini terjadi perubahan neutron menjadi proton dengan memancarkan elektron negatif atau negatron.
Contoh :
(2) Peluruhan positron
Contoh :
(3) Penangkapan elektron. Proses ini jarang terjadi pada isotop alam, tetapi terjadi pada radionuklida buatan.
Contoh :
c) Peluruhan gamma
Proses ini seringkali disebut transisi isomer. Pada peluruhan sinar gamma tidak dihasilkan unsur gres alasannya sinar gamma merupakan energi foton yang tidak bermassa dan tidak bermuatan.
2) Pembelahan Spontan
Proses ini hanya terjadi pada nuklida-nuklida yang nomor atomnya besar dan membelah secara impulsif menjadi dua nuklida yang massanya berbeda.
3) Mengalami Transmutasi Inti
Pada tahun 1919, Rutherford berhasil menembak gas nitrogen dengan partikel alfa dan menghasilkan hidrogen dan oksigen.
Reaksi ini merupakan transmutasi buatan pertama yaitu perubahan suatu unsur menjadi unsur lain.
Pada tahun 1934, Irene Joliot Curie, putri Marie Curie, berhasil menciptakan atom fosfor yang bersifat radioaktif dengan menembakkan aluminium dengan sinar alfa yang berasal dari polonium.
Anda kini sudah mengetahui Sifat Fisika dan Kimia Unsur Radioaktif. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Sukmanawati, W. 2009. Kimia 3 : Untuk SMA/ MA Kelas XII. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 266.