Kelimpahan, Pembuatan, Kegunaan Unsur Transisi, Dampak Negatif, Bahaya, Kimia - Kamu telah mempelajari fisika-dan-kimia-unsur-transisi-periode-ke-4-keempat" target="_blank">sifat-sifat unsur transisi, kini tahukah kau kelimpahan dari fisika-dan-kimia-unsur-transisi-periode-ke-4-keempat" target="_blank">unsur-unsur transisi periode ke 4 tersebut di alam ini? Mari kita pelajari kelimpahan beberapa transisi di alam ini.
1. fisika-dan-kimia-unsur-transisi-periode-ke-4-keempat" target="_blank">Kelimpahan Unsur Transisi
1.1. Kromium (Cr)
Kromium merupakan logam keras berwarna putih. Ditemukan di alam sebagai bijih krom besi, yaitu kromit (FeCr2O4) yang banyak ditemukan di Sumatra Barat, Sumatra Utara, Kalimantan Barat, Kalimantan Selatan, Sulawesi Selatan, dan Papua.
1.2. Ferrum (Fe)
Ferrum atau besi yakni logam yang paling murah di antara logam-logam yang dikenal manusia. Besi berwarna putih , cukup lunak, dan bersifat magnetik. Besi berada di alam sebagai bijih besi. Bijih utamanya hematit (Fe2O3), limotit (HFeO2), siderit (FeCO3), pirit (FeS2), dan ilminit (FeTiO3). Bijih besi tersebar di kawasan Kalimantan Barat, Sumatera Barat, Sumatera Selatan, dan Sulawesi Tengah.
1.3. Cuprum (Cu)
Cuprum atau tembaga merupakan logam transisi berwarna merah-cokelat, berupa logam lunak tetapi kuat. Ditemukan di alam pada batuan tertentu. Senyawaan tembaga, antara lain pirit tembaga, (CuFe)S2 dan malasit, CuCO3.Cu(OH)2. Potensi tembaga terbesar di Indonesia terdapat di Papua, Jawa Barat, Sulawesi Utara, dan Sulawesi Selatan.
1.4. Titanium (Ti)
Titanium merupakan logam kesembilan terbanyak, mencakup 0,6% kerak bumi.
1.5. Vanadium (V)
Vanadium merupakan unsur yang cukup banyak terdapat (0,02% kerak bumi) dan ditemukan pada beberapa macam bijih. Salah satu bijih yang penting secara komersil ialah V2S5.
1.6. Mangan (Mn)
Mangan berupa logam yang keras dan rapuh. Bijih mangan yang utama yakni pirolusit, MnO2. Potensi mangan terdapat di Pulau Sumatra, Kepulauan Riau, Pulau Jawa, Pulau Kalimantan, Pulau Sulawesi, Nusa Tenggara, Maluku, dan Papua.
2. fisika-dan-kimia-unsur-transisi-periode-ke-4-keempat" target="_blank">Kegunaan Unsur Transisi
Unsur-unsur transisi mempunyai banyak kegunaan. Berikut merupakan beberapa unsur transisi dan kegunaannya.
2.1. Kromium (Cr)
Penggunaan kromium yang sangat populer yakni penyepuhan kromium (chromium plating). Efek penting dalam penyepuhan ini yakni dekoratif dan sifat kekerasan. Lapisan kromium itu indah, tidak kusam, dan memberi efek tahan panas, tahan pakai, tahan korosi serta bersifat keras. Penyepuhan kromium banyak dipakai pada peralatan sehari-hari, dan kendaraan bermotor.
Elektrolit dibuat dengan melarutkan kromium (VI) oksida, CrO3, dalam air sehingga membentuk asam dikromat H2Cr2O7. Dalam penyepuhan ini sebagai katalis ditambah sedikit H2SO4 untuk mempercepat pelapisan kromium. Proses penyepuhan ini berbeda dari penyepuhan lainnya. Sebagai anode tidak dipakai logam kromium lantaran logam ini gampang melarut dalam larutan asam. Anode yang dipakai yakni aliasi Pb–Sn, yang tidak melarut dalam asam kromat. Reaksi pada elektrode sanggup ditulis sebagai berikut.
| Anode | : | 2H2O(l) → O2(g) + 4H+(aq) + 4e- |
| Katode | : | Cr2O72-(aq) + 14H+(aq) + 12e- → 2Cr(s) + 7H2O(l) |
Ke dalam wadah elektrolisis selalu ditambahkan CrO3 untuk menjaga konsentrasi kromium biar selalu tetap. Kegunaan kromium yang lain yaitu dalam pembuatan stainless steel. Senyawa kromium mempunyai warna yang sangat menarik, oleh lantaran itu dipakai sebagai pigmen mirip kuning krom (timbal (II) kromat) dan hijau krom (kromium (III) oksida). Suatu senyawa kromium yang indah sekali yakni jamrud (emerald). Batu permata ini terbentuk bila sebagian ion aluminium dalam mineral beril, Be3Al2(Si6O18) diganti oleh ion kromium (III).
2.2. Ferrum (Fe)
Manfaat ferrum atau besi antara lain sebagai materi utama pembuatan baja. Adapun manfaat baja yakni mirip pada tabel berikut ini.
Tabel 1. Komposisi Baja dan Kegunaannya
| Macam Baja | Komposisi | Sifat | Kegunaan |
| baja sedang | 0,009 – 0,2% C | mudah dibuat | badan kendaraan beroda empat |
| 0,05 – 1,0% Mn | jarum | ||
| 0,2 – 0,75% Si | pipa | ||
| baja berkadar | 0,4 – 0,9% C | keras | perkakas |
| karbon tinggi | 0,5 – 1,0% Mn 0,2 – 0,75% Si | | paku, pelat |
| stainless steel | 0,2 – 0,4% C | tahan korosi | pisau |
| 18% Cr 8% Ni | perkakas | ||
| baja mangan | 0,4 – 0,9% C 13% Mn | kuat dan keras | per |
| baja wolfarm | 0,4 – 0,9% C | sangat keras | ujung alat |
| 5% W | pemotong |
2.3. Cuprum (Cu)
Cuprum atau tembaga banyak dipakai sebagai kabel jaringan listrik lantaran sifatnya yang menghantarkan listrik. Tembaga juga dipakai untuk menciptakan pipa leding. Alloy tembaga dan emas dipakai untuk menciptakan perhiasan.
2.4. Titanium (Ti)
Titanium mempunyai kerapatan rendah, kekuatan struktur yang tinggi, dan tahan terhadap korosi. Oleh lantaran sifat inilah titanium banyak dipakai pada industri pesawat terbang dan industri kimia sebagai pipa, cuilan pompa dan ember pereaksi. Titanium tetraklorida, TiCl4 merupakan senyawa titanium terpenting. Senyawa ini merupakan materi baku untuk menciptakan senyawa Ti yang lain, memegang peranan penting pada metalurgi titanium dan dipakai dalam pembuatan katalis untuk produksi polietilena dan plastik lainnya.
2.5. Vanadium (V)
Sekitar 80% produksi vanadium dipakai untuk pembuatan baja. Baja yang mengandung vanadium dipakai pada peralatan yang membutuhkan kekuatan dan kelenturan, mirip pegas dan alat-alat mesin berkecepatan tinggi.
2.6. Mangan (Mn)
Pada produksi baja, Mn berpartisipasi pada pemurnian besi melalui reaksi dengan sulfur dan oksigen dengan memindahkannya melalui pembentukan terak. Fungsi yang lain yakni untuk meningkatkan kekerasan baja. Baja yang mengandung Mn dengan proporsi besar bersifat sangat keras dan tahan lama. Oleh lantaran itu dipakai dalam kereta api dan mesin-mesin buldoser.
Kalium permanganat, KMnO4 merupakan zat pengoksida yang penting dalam analisis kimia, biasanya dipakai pada titrasi larutan asam di mana senyawa tersebut direduksi menjadi Mn2+. Pada kimia organik MnO4– digunakan untuk mengoksidasi alkohol dan hidrokarbon tidak jenuh. Adapun mangan dioksida, MnO2, dipakai pada sel kering, pada beling dan lapisan keramik, serta sebagai katalis.
2.7. Zink (Zn)
Zink dipakai untuk melapisi besi dan baja untuk mencegah karat. Zink juga dipakai dalam alloy contohnya brazo (tembaga dan zink).
3. fisika-dan-kimia-unsur-transisi-periode-ke-4-keempat" target="_blank">Cara Pembuatan Unsur Transisi
Unsur-unsur transisi berada di alam dalam bentuk senyawaan. Bagaimana cara untuk mendapat unsur-unsur transisi tersebut? Mari kita pelajari cara mendapat beberapa unsur transisi berikut ini.
3.1. Kromium (Cr)
Dalam bidang industri, kromium diharapkan dalam dua bentuk, yaitu kromium murni, dan aliansi besi-kromium yang disebut ferokromium. Unsur krom sanggup kita peroleh dengan cara mengekstraksi bijihnya.
Langkah-langkah dalam ekstraksi unsur krom dari bijihnya yakni mirip berikut.
a. Kromium (III) dalam bijih diubah menjadi dikromat (VI)
b. Reduksi Cr (VI) menjadi Cr (III)
c. Reduksi kromium (III) oksida dengan aluminium (reaksi termit)
Hasil ekstrasi ini diperoleh logam kromium dengan kemurnian 97% – 99%.
Adapun ferokromium diperoleh dengan mereduksi bijih dengan kokas atau silikon dalam tanur listrik.
3.2. Ferrum (Fe)
Ferrum atau besi sanggup diperoleh dengan cara mengekstrasi bijihnya dalam tanur hembus atau tanur tinggi. Bahan baku yang diharapkan dimasukkan dalam tanur tinggi yaitu bijih besi, karbon, dan kerikil kapur (CaCO3). Proses tanur hembus yakni reduksi bijih besi dengan karbonmonoksida yang dihasilkan dari kokas dan udara yang dihembuskan dari dasar tanur.
C(s) + O2(g) → CO2(g) : ΔH = -394 kJ mo1-1
Selanjutnya CO2 yang terbentuk bereaksi dengan karbon yang berlebih membentuk CO.
CO2(g) + C(s) → 2CO(g) : ΔH = +172 kJ mo1-1
Karbon monoksida mereduksi bijih besi menjadi besi dengan tahapan reaksi mirip berikut.
3FeO3(s) + CO(g) → 2Fe3O4(s) + CO2(g)
Fe3O4(s) + CO(g) → 3FeO(s) + CO2(g)
FeO(s) + CO(g) → Fe(s) + CO2(g)
Reaksi-reaksi tersebut sanggup ditulis mirip berikut.
Fe2O3(s) + 3CO(g) ⇌ 2Fe(s) + 3CO2(g) (reaksi kesetimbangan)
Akhirnya besi akan meleleh dan jatuh di cuilan tanur yang lebih panas. Adapun kerikil kapur (CaCO3) terurai pada suhu tinggi menghasilkan kalsium oksida.
CaCO3(s) → CaO(l) + CO2(g)
Di cuilan bawah, kalsium oksida bereaksi dengan zat pengotor mirip silikon (IV) oksida (silika) menghasilkan kalsium silikat.
CaO(l) + SiO2(s) → CaSiO3(s)
Tanur bekerja terus menerus. Campuran pereaksi dimasukkan dari puncak tanur dalam selang waktu yang teratur, bergerak ke bawah hingga lapisan terbawah yang panas keputih-putihan. Suhu pada dasar tanur cukup panas sehingga melelehkan besi dan terak (zat pengotor yang telah terikat kalsium) yang terdapat sebagai lapisan yang tak tercampur di dasar tanur. Leburan terak mengapung di atas permukaan lelehan besi.
Besi yang dihasilkan dari tanur hembus masih mengandung zat pengotor mirip karbon, silikon, sulfur dan fosfor. Zat-zat pengotor ini menimbulkan besi lebih getas, besi ini disebut besi tuang. Komposisi besi tuang bervariasi bergantung pada sumbernya.
Baja merupakan suatu alloy besi. Baja dibuat dari besi tuang. Setelah zat pengotor dalam besi dihilangkan, kemudian ditambah sejumlah karbon dan unsur lain yang memperlihatkan sifat khas pada baja itu.
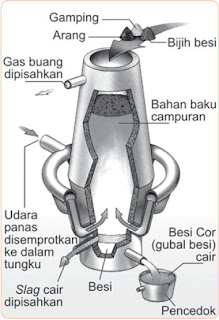 |
| Gambar 1. Tungku Bassemer. |
Pada tahun 1856, Henry Bassemer dari Inggris menemukan metode menciptakan baja dari besi. Alat yang diharapkan disebut tungku Bassemer. Tungku tersebut dilapisi pelapis tahan api. Leburan besi dituang ke dalam tungku Bassemer, kemudian dihembuskan oksigen ke leburan. Karbon, sulfur dan fosfor keluar sebagai oksida berupa gas, sedangkan silikon oksida membentuk terak di atas besi. Setelah terak dipisahkan, pada leburan besi ditambah karbon, mangan dan unsur lain. Kadar karbon dalam baja berkisar antara 0,09% – 0,9%.
3.3. Titanium (Ti)
Langkah awal produksi Ti yakni pengubahan bijih (TiO2) rutil menjadi TiCl4. TiCl4 yang sudah dimurnikan selanjutnya direduksi menjadi Ti dengan memakai zat pereduksi yang baik, proses isi disebut proses Kroll memakai Mg. Reaksi dilakukan pada tabung baja. MgCl2 dipindahkan dan dielektrolisis menjadi Mg dan Cl2, keduanya kemudian didaurulangkan. Ti didapatkan sebagai padatan yang disebut sepon. Sepon harus diolah lagi dan dicampur dengan logam lain sebelum sanggup digunakan. Salah satu problem pengembangan Ti secara komersial ialah perencanaan teknik metalurgi gres untuk pembuatan logam Ti di pabrik.
3.4. Mangan (Mn)
Sumber utama senyawa mangan ialah MnO2. Jika MnO2 dipanaskan dengan penambahan alkali dan zat pengoksidasi, maka akan terbentuk garam manganat.
3MnO2(s) + 6KOH(l) + KClO3(l) → 3K2MnO4(aq) + KCl(l) + 3H2O(l)
K2MnO4 diekstraksi dari materi adonan dalam air, dan sanggup dioksidasi menjadi KMnO4 (misalnya dengan Cl2 sebagai zat pengoksidasi).
Nodul Mangan (Manganese Nodules), benda ini mirip batuan dan ditemukan di dasar laut. Nodul mangan tersusun oleh lapisan Mn dan Fe oksida, dengan sejumlah kecil logam lain mirip Co, Cu dan Ni. Nodul biasanya berbentuk bundar dengan diameter antara beberapa milimeter hingga sekitar 15 cm. Benda ini diduga tumbuh dengan kecepatan beberapa milimeter per sejuta tahun. Telah dilaporkan bahwa organisme bahari mungkin berperan dalam pembentukannya. Diperkirakan jumlah nodul ini sangat besar, mungkin bermilyar ton. Namun, masih banyak, tantangan untuk membuatkan nodul mangan sebagai materi baku mangan. Banyak metode harus disempurnakan untuk menjelajah dasar laut, mengeruk nodul, dan membawanya dari kedalaman air laut. Dan juga, diharapkan proses metalurgi gres untuk mengekstrak logam yang diinginkan. Cadangan terbesar nodul mangan yang diketahui berada di kawasan Kepulauan Hawai tenggara.
3.5. Zink (Zn)
Untuk mendapat zink dilakukan dengan ekstraksi yaitu dengan memanggang bijihnya untuk menciptakan ZnO kemudian direduksi dengan memanaskannya dengan arang.
4. fisika-dan-kimia-unsur-transisi-periode-ke-4-keempat" target="_blank">Dampak Negatif Unsur Transisi
Pada dasarnya dampak dari unsur transisi disebabkan adanya pemanfaatan unsur transisi. Makara selain bermanfaat ternyata juga menjadikan problem lingkungan. Adapun dampak negatif dari pemanfaatan unsur transisi antara lain, sebagai berikut.
4.1. Limbah Fe
Pada pengolahan logam besi, bila limbahnya dibuang ke sungai sanggup menimbulkan pertumbuhan fitoplankton yang tidak terkendali. Hal ini menimbulkan penurunan kadar oksigen dalam air sehingga akan mengganggu pertumbuhan ikan dan binatang air lainnya.
4.2. Cr dalam penyamakan kulit
Krom dipakai dalam penyamakan kulit untuk mencegah mengerutnya materi sewaktu pencucian. Krom ini sangat beracun dan menimbulkan kanker.
4.3. Mn dalam pengelasan dan pembuatan baja
Pada pengelasan dan pembuatan baja dengan logam Mn akan dihasilkan suatu asap dalam jumlah yang banyak. Asap ini bersifat racun dan sanggup mengganggu sistem saraf pusat.
4.4. Cu
Pada penambangan tembaga, akan terbuang pasir sisa yang masih mengandung logam Cu. Jika pasir sisa ini dibuang ke perairan maka akan membahayakan organisme-organisme di perairan tersebut.
Anda kini sudah mengetahui Kelimpahan Unsur Transisi, Pembuatan Unsur Transisi, Kegunaan Unsur Transisi, dan Dampak Negatif Unsur Transisi. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Sukmanawati, W. 2009. Kimia 3 : Untuk SMA/ MA Kelas XII. Pusat Perbukuan, Departemen Pendidikan Nasional, Jakarta, p. 266.





