 |
| Indikator Senyawa Asam dan Basa |
Indikator, Derajat Keasaman, dan Tetapan Kesetimbangan Air Lengkap
Dalam pembahasan asam basa ini saya akan membaginya menjadi beberapa sub sajian ibarat indikator asam basa, derajat keasaman asam basa dan tetapan kesetimbangan air asam basa. Berikut klarifikasi selengkapnya:
Baca juga : soal-rumus-empiris-dan-rumus" target="_blank">Contoh Soal Rumus Empiris dan Rumus Molekul Beserta Pembahasan
Indikator Asam Basa
Pengertian indikator ialah zat yang sanggup memperlihatkan petunjuk sebuah larutan mempunyai sifat asam ataupun basa. Dalam mengukur pH asam basa tersebut intinya sanggup memakai indikator tersebut ataupun memakai perhitungan tertentu. Indikator asam basa sendiri sanggup dilakukan dengan cara tertentu. Maka dari itu untuk mengetahui zat yang sifatnya basa atau asam dihentikan dengan cara dipegang ataupun dicicipi. Hal ini dikarenakan cara cara tersebut salah alasannya yaitu membahayakan. Misalnya air aki (accu zuur) sering dipakai dalam kehidupan sehari hari dengan kandungan H2SO4 (asam sulfat) di dalamnya. Jika asam sulfat tersebut populer kulit maka akan menimbulkan luka bakar atau melepuh dan menimbulkan kebutaan apabila mengenai mata.
Selain itu adapula basa untuk membersihkan kanal air kolam basuh dengan kandungan NaOH (Natrium Hidroksida). Jika NaOH terkena kulit atau tangan maka akan menciptakan iritasi, terluka, ataupun gatal gatal. Nah untuk mengetahui kadar sifat dalam larutan tersebut memakai indikator asam basa ini. Dengan zat indikator tersebut kita sanggup mengetahui sifat larutan dengan benar, baik asam ataupun basa. Untuk memilih sifat larutan memakai indikator sanggup dilakukan dengan dua cara yakni memakai larutan indikator dan memakai kertas lakmus. Berikut penjelasannya yaitu:
Menggunakan Kertas Lakmus
Jenis indikator asam basa yang pertama sanggup berupa kertas lakmus. Kertas lakmus sebagai indikator di laboratorium kimia yang sering dipakai sanggup berupa kertas lakmus biru dan kertas lakmus merah. Hasil percobaan kertas lakmus ini sanggup ditujukan pada larutan cuka dapur, air kapur dan larutan air suling. Berikut tabel hasil percobaan pada kertas lakmus biru dan merah yaitu:
 |
| Tabel Indikator Asam dan Basa Menggunakan Kertas Lakmus |
Larutan Indikator
Jenis indikator asam basa selanjutnya sanggup berupa larutan indikator. Di laboratorium kimia sering memakai larutan indikator ibarat metil merah, bromtimol biru, fenolftalein, dan metil jingga. Berikut tabel hasil pengujian larutan asam dan larutan basa memakai larutan indikator ibarat di bawah ini:
Baca juga : soal-rumus-empiris-dan-rumus" target="_blank">Rumus Empiris dan Rumus Molekul Beserta Contoh Soal
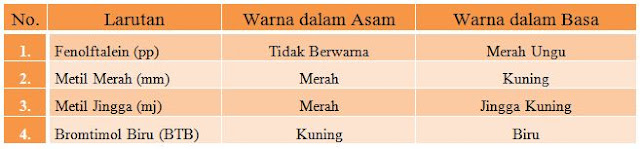 |
| Tabel Indikator Asam dan Basa Menggunakan Larutan Indikator |
Untuk mengetahui indikator asam dan basa dalam sebuah larutan tidak hanya memakai dua cara diatas. Namun masih adapula beberapa cara mengetahui sebuah larutan bersifat asam ataupun basa memakai langkah langkah di bawah ini:
Menggunakan Indikator Universal
Pengertian indikator universal ialah kombinasi dari beberapa faktor. Indikator asam basa tersebut memakai larutan maupun kertas serap yang berupa kotak lengkap dengan peta warna. Kertas serap yang dipakai sebagai indikator intinya mempunyai cara kerja yang cukup sederhana yaitu cukup menetesi atau mencelupkannya ke larutan yang akan diukur pH nya. Setelah itu memakai peta warna yang tersedia untuk membandingkan terjadinya perubahan warna.
Menggunakan pH Meter
Pengertian pH meter ialah alat yang mempunyai ketelitian sangat tinggi dalam mengukur pH larutan. Indikator asam basa yang memakai pH meter ini diwujudkan dalam bentuk temperatur dengan angka angka desimalnya. Cara kerja pH meter memang cukup sederhana yaitu dicelupkan pada larutan yang akan diukur pH nya. Setelah itu akan muncul angka pada jarum skala pH meter, kemudian kita tinggal membaca angka yang ditunjukkan saja.
Indikator Alami
Indikator alami sanggup dipakai sebagai indikator asam basa pada sebuah larutan selain memakai larutan indikator, pH meter, kertas lakmus dan indikator universal. Indikator alami yang dipakai untuk mengetahui senyawa asam atau basa tersebut sanggup berupa kunyit, bunga sepatu, kol merah dan sebagainya.
Derajat Keasaman (pH) Asam Basa
Setelah menjelaskan ihwal indikator asam basa, selanjutnya saya akan membahas ihwal derajat keasaman asam basa. Dalam sebuah zat terdapat bilangan yang menggambarkan jumlah ion H+ (Hidrogen) dan jumlah ion OH- (Hidroksil) berjulukan derajat keasaman dan kebasaan. Derajat keasaman dan kebasaan pada suatu zat tersebut mempunyai nilai yang sesuai dengan jumlah ion OH- dan H+ di dalam air. Jika di dalam air terdapat ion H+ yang semakin banyak dan ion OH- semakin sedikit jumlahnya, maka zat tersebut akan semakin asam. Sedangkan bila di dalam air terdapat ion H+ yang semakin sedikit jumlahnya dan ion OH- semakin banyak, maka zat tersebut akan semakin basa. Di dalam air terdapat jumlah ion OH- dan H+ yang sanggup dinyatakan dalam bentuk pOH ataupun pH.
Baca juga : soal-rumus-empiris-dan-rumus" target="_blank">Tekanan Osmosis (Pengertian, Rumus, Proses Terjadi, dan Contohnya)
Biasanya derajat keasaman asam basa sanggup ditentukan memakai skala pH. Skala pH tersebut sanggup menujukkan derajat keasaman sebuah zat (pH) dengan skala sekitar 0 - 14 meter. Setelah melaksanakan langkah langkah indikator asam basa, selanjutnya tinggal melaksanakan langkah langkah mengetahui derajat keasaman sebuah zat tersebut. Berikut beberapa skala pH untuk memilih sifat asam atau basa sebuah zat yaitu meliputi:
- Larutan bersifat asam bila pH kurang dari 7 (pH < 7).
- Larutan bersifat netral bila pH sama dengan 7 (pH = 7).
- Larutan bersifat basa bila pH lebih dari 7 (pH > 7).
Suatu zat akan semakin asam bila nilai pH semakin kecil, sedangkan suatu zat akan semakin basa bila nilai pH semakin besar. Di bawah ini terdapat rumus pH dan pOH untuk memilih nilainya yaitu sebagai berikut:
 |
| Rumus Menentukan Nilai pH dan pOH |
Tetapan Kesetimbangan Air (Kw)
Setelah menjelaskan ihwal indikator asam basa dan derajat keasaman asam basa. Selanjutya saya akan membahas ihwal tetapan kesetimbangan air atau Kw. Zat elektrolit ialah hasil pengukuran daya hantar listrik dalam air murni yang peka memakai ampermeter. Namun zat ini mempunyai hantaran listrik dan elektrolit yang cukup lemah. Hal ini memperlihatkan adanya hasil ionisasi air melalui hantaran yang ditunjukkan dalam bentuk ion ior di air murni. Adapun persamaan ionisasi airnya yaitu sebagai berikut:
 |
| Persamaan Ionisasi Air |
Namun tetapan kesetimbangan air sanggup diketahui nilainya saat dalam keadaan setimbang memakai rumus di bawah ini:
 |
| Rumus Tetapan Kesetimbangan Air |
Dalam air murni terdapat persamaan besar antara konsentrasi ion H+ dengan ion OH- sehingga sifat air yaitu netral. Jika asam ditambahkan ke air maka keadaannya akan menciptakan ion H+ terlepas dari asam sehingga akan bertambah banyak konsenrasi ion H+ nya. Dengan begitu kesetimbangan air akan terganggu alasannya yaitu berkurangnya konsentrasi ion H- dan harga Kw tetap. Namun apabila di dalamnya ditambah air, maka akan terjadi ionisasi basa yang menciptakan ion OH- terlepas sehingga dalam air akan lebih besar konsentrasi OH- nya serta berkurangnya konsentrasi ion H+.
Sekian klarifikasi mengenai indikator asam basa, derajat keasaman asam basa dan tetapan kesetimbangan air lengkap. Sebuah larutan sanggup diketahui apakah sifatnya asam atau basa memakai beberapa cara ibarat memakai kertas lakmus, larutan indikator, indikator universal, pH meter dan indikator alami. Semoga artikel ini sanggup menambah ilmu anda dan terima kasih telah berkunjung di blog ini.





